Dose 1
0,5 ml
Administreres i
måned 0 (dag 1)
Dose 2
0,5 ml
Administreres i
måned 3 (dag 91)
Effekt
Oppnås 1 måned
etter den andre
dosen (dag 121)
Beskytt pasientene dine ved å vaksinere i god tid før avreise
Kvalifiserte pasienter skal vaksineres med to doser av Qdenga™-vaksinen med tre måneders mellomrom [1]
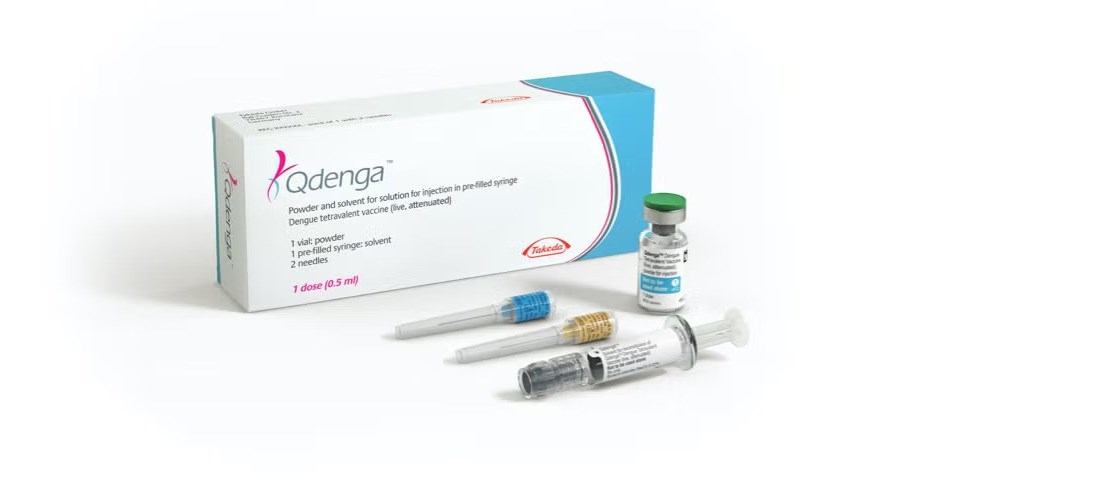

QdengaTM er indisert for forebygging av dengue-sykdom forårsaket av alle denguevirusserotyper hos personer fra 4 år [1]

Oppbevar QdengaTM i kjøleskap (2-8 °C);skal ikke fryses Holdbarhet: 18 måneder [1]
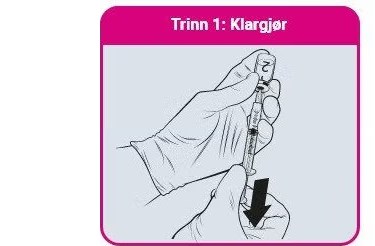
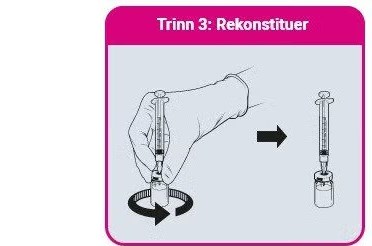
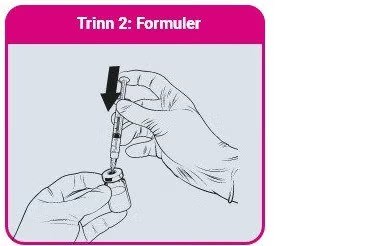
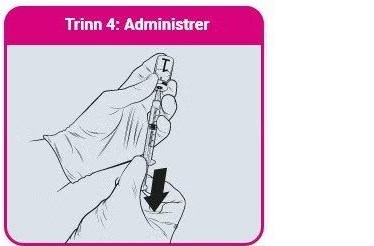
- QdengaTM må alltid administreres i henhold til din lokale godkjente produktinformasjon
- QdengaTM er tilgjengelig som pulver og oppløsning for injeksjon, med eller uten en forhåndsfylt sprøyte (det er ikke sikkert at alle pakningsstørrelser markedsføres i alle regioner) [1]
- QdengaTM skal rekonstitueres med fortynningsmiddel før administrasjon og brukes umiddelbart [1]
- QdengaTM må brukes innen 2 timer hvis det ikke brukes umiddelbart [1]
- QdengaTM må brukes innen 2 timer hvis det ikke brukes umiddelbart [1]
- QdengaTM skal administreres ved subkutan injeksjon, fortrinnsvis i overarmen i deltoidregionen [1]
- Behovet for en boosterdose er ikke etablert [1]
- Anbefalt nålstørrelse er 23G (trinn 1-3). Anbefalt nålstørrelse for vaksineadministrasjon er 25G (trinn 4).
Utvikling
Takeda har mer enn 70 års erfaring med vaksineutvikling og -produksjon [2]
QdengaTMer utviklet og prepareres iht. cGMP-betingelser i samsvar med de nyeste regulatoriske kravene [3], [4]

.

.

.

DEN-2-virus ble isolert fra naturen og attenuert. Deretter ble de andre kiremiske virusene DEN-1, DEN-2 og DEN-4 utviklet ved bruk av rekombinante teknikker og det attenuerte DEN-2-viruset [4]
DENV-2-stammen attenueres, og ved bruk av rekombinasjonsteknikker dannes de andre tre kimeriske virusene ved å erstatte prM- og E-proteingenene fra DENV-1, -3 og -4 i DENV-2-hovedkjeden [3]
Andre ikke-aktive ingredienser, inkludert stabiliseringsmidler, tilsettes slik at formuleringen blir levedyktig [3]
Kvaliteten og kraften (dvs. den biologiske aktiviteten) til hver levende, attenuert, tetravalent formulering kontrolleres for å bidra til å sikre kvaliteten, integriteten og sikkerheten for hvert produkt
I hvilke land er Qdenga tilgjengelig?
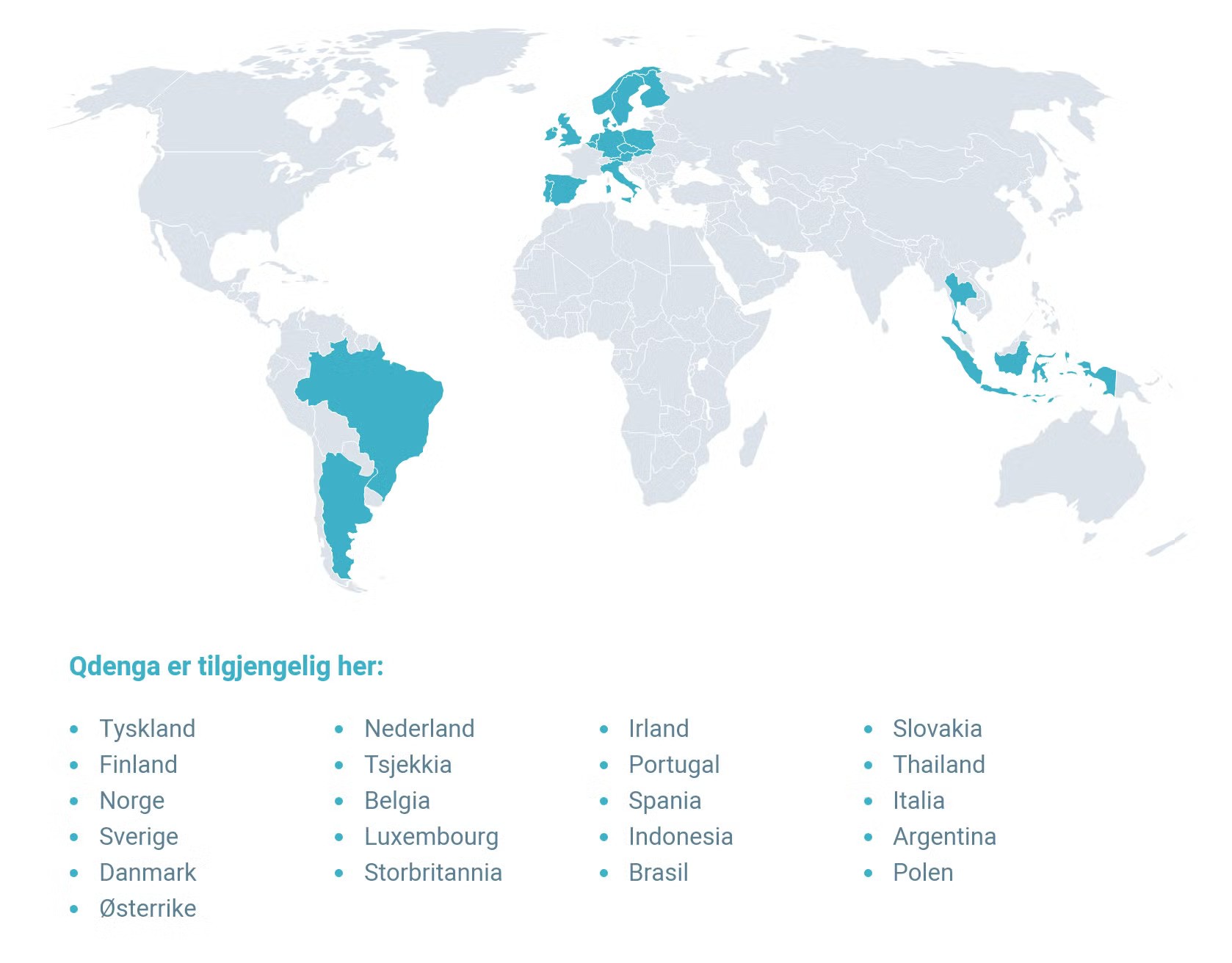
cGMP, gjeldende god produksjonspraksis; DENV, denguevirus.
Referanser
-
1. [SPC] QdengaTM Summary of Product Characteristics (12/2022)
-
2. [TAKPR] Takeda Newsroom. Takeda unveils new dengue vaccine manufacturing plant in Germany. November 05, 2019.
https://www.takedavaccines.com/news/release/takeda-unveils-new-dengue-vaccine-manufacturing-plant-in-germany2/ Retrieved May 2021. -
3. [OSO15] Osorio JE, et al. Vaccine. 2015;33(50):7112-7120.
-
4. [HUA13] Huang CY-H, et al. PLoS Negl Trop Dis. 2013;7(5):e2243.